УЗИ предсказывает успех лечения рака печени
Ученые разработали программное обеспечение для ультразвукового обследования с контрастным усилением (CEUS), которое может точно предсказать, какие пациенты с распространенным типом рака печени будут отвечать на транскатетерную артериальную химиоэмболизацию (TACE), говорится в результатах исследований, опубликованных в журнале Ultrasound in Medicine and Biology.
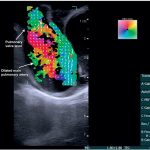
Специально созданное программное обеспечение улучшает визуализацию кровеносных сосудов опухоли печени у пациентов с гепатоцеллюлярной карциномой (ГЦК), одним из самых распространенных типов рака. Путем количественной оценки характеристик кровеносных сосудов опухоли исследователи смогли определить, какие пациенты с ГЦК с большей вероятностью будут отвечать на ТАСЕ, чем на другие методы лечения.
«Сложность сосудистой сети опухоли может негативно влиять на артериальную доставку гранул, выделяющих лекарственный препарат во время процедуры ТАСЕ, – пишут авторы исследования. – Таким образом, количественная оценка сосудистой сети опухолей может предоставить важную информацию врачам во время планирования лечения».
Обработка изображений, извлечение данных и моделирование
Процедура ТАСЕ использует катетер для доставки химиотерапевтических препаратов в сосудистую сеть опухоли. В случае успеха ТАСЕ полностью блокирует кровеносные сосуды опухоли, но до 75% опухолей имеют остаточный кровоток, требующий повторного лечения или иной формы терапии.
Ответ пациента на ТАСЕ, как правило, проверяется через 4-6 недель после лечения с помощью МРТ или КТ с контрастным усилением. Но авторы исследования выдвинули предположение, что УЗИ с контрастным усилением может работать лучше – не только для мониторинга ответа пациентов на лечение, но и для визуализации сосудистой сети опухоли до его начала.
Они проверили свою гипотезу, используя данные визуализации 36 пациентов с ГЦК, принявших участие в клинических испытаниях, оценивающих эффективность 2D- и 4D-CEUS для ТАСЕ. Для целей исследования, опытный врач УЗИ – диагностики проводил CEUS сканирование пациентов трижды – до и после лечения.
Авторы разработали специальный MATLAB скрипт обработки CEUS изображений для лучшей визуализации сосудов. Они применяли это программное обеспечение только для обработки данных визуализации первого CEUS сканирования пациентов, проводимого до начала процедуры ТАСЕ.
На основании обработанных изображений авторы выделили шесть уникальных характеристик:
- соотношение сосудов к ткани,
- число бифуркаций,
- количество сосудов,
- средний диаметр сосудов,
- средняя длина судов,
- извилистость сосудов.
Они создали модели, использующие морфологические признаки для прогнозирования эффективности лечения методом ТАСЕ, и сравнили прогнозы моделей с фактическими результатами лечения пациентов. Из 33 пациентов 19 человек имели полный ответ на ТАСЕ, в то время как у остальных был остаточный кровоток. Пациенты с неполным ответом на ТАСЕ имели большее количество сосудов и бифуркаций на изображениях первичного CEUS сканирования, отмечают авторы.
Точность до 86%
Анализ данных показал, что диаметр сосудов являлся самым слабым прогностическим показателем на успех ТАСЕ терапии, в то время как соотношение сосудов к ткани, количество сосудов и количество бифуркаций имели самые сильные способности прогнозирования.
Модель, которая использовала все шесть морфологических признаков, имела только 52% точность, но точность возрастала до 72% у модели без самого слабого прогностического фактора (диаметр сосудов). Когда исследователи задействовали только самые сильные прогностические факторы (соотношение сосудов к ткани, число бифуркаций и количество сосудов), точность подскочила до 86% с чувствительностью 89% и специфичностью 82%.
«В целом эти показатели эффективности подтвердили, что наша модель могла сделать надежные прогнозы относительно ответа ГЦК на ТАСЕ до начала лечения», – написали авторы.
Перспективы для персонализированного лечения рака
Авторы предположили, что характеристики сосудов могут точно предсказывать ответ на ТАСЕ терапию, потому что более сложные сосудистые сети негативно влияют на доставку лекарственных препаратов. Сложные сосудистые сети также могут быть признаком более агрессивной опухоли и могут говорить об опухолях, которые лучше реагируют на трансартериальную радиоэмболизацю (TARE), чем на TACE.
Для подтверждения эффективности программного обеспечения для обработки изображений и прогностической модели необходимо проведение дополнительных исследований с большим числом участников. Но в случае успешного подтверждения, CEUS визуализация может стать бесценным инструментом для лечения рака, использующим персонализированный подход для пациентов с ГЦК.
«Разработанный инновационный метод визуализации и обработки изображений CEUS одновременно определяет морфологические особенности сосудистой сети опухоли и предсказывает ответ ГЦК на ТАСЕ терапию, – пишут в заключении авторы. – Внедрение надежного метода прогнозирования ответа на ТАСЕ поможет сделать планирование более эффективным и даст больше персонализированных стратегий лечения пациентов».
Оригинал новости можно прочитать здесь