Тераностика: оружие будущего против рака
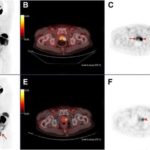
Радиотераностика – новейший метод лечения рака «изнутри» – использует молекулы, способные безопасно переносить радиоактивные изотопы внутри человеческих тканей. Эти молекулы помогают врачам получить более детальное изображения опухолей, а затем – уничтожить раковые клетки максимально прицельно и эффективно.
В 2011 году область применения радиотераностики ограничивалась использованием 131I-йодида натрия для лечения рака щитовидной железы, 131I-Тозитумомаба (BEXXAR) и 90Y-Ибритумомаба тиуксетана (Zevalin) – для лечения неходжкинской лимфомы, а также солей самария-153 или стронция-89 для проведения некоторых лучевых паллиативных процедур, облегчающих боли.
Но десять лет спустя поток препаратов с мечеными радиоизотопами, проходящих клинические испытания, вырос благодаря двум значительным событиям. Во-первых, началось промышленное использование очень интересного бета-излучающего радионуклида, а именно – лютеция-177. И, во-вторых, тераностика стала вызывать все больший интерес у ученых и врачей.
Концепция радиотераностики, ранее реализованная в разработке и внедрении Bexxar и Zevalin, была основана на простом последовательном использовании молекулы – сначала для диагностики, затем для лечения заболевания. В радиотераниостике эта технология позволяет использовать одну и ту же молекулу для воздействия на конкретную ткань или на биологический механизм (вектор).
На первом этапе к молекуле прикрепляется гамма- или позитронный излучатель, который позволяет провести соответственно диагностику SPECТ (однофотонная эмиссионная компьютерная томография) или PET (позитронно-эмиссионная томография). В случае положительного биораспределения (выявления на снимках раковых клеток) та же молекула, в которой радионуклид для лучевой диагностики заменен на бета или альфа-радионуклид, излучающий ядерные частицы, используется для разрушения ДНК уже обнаруженных клеточных масс. Другими словами, радиотераностика – это пара молекул, помогающих увидеть болезнь, выбрать метод лечения и уничтожить опухолевое образование. Технология, объединяющая и диагностику, и лечение, позволяет безошибочно отбирать пациентов, которые практически гарантировано будут иметь положительный ответ на терапию соответствующим методом.
Десять лет спустя концепция радиотераностики расширилась. Теперь она объединяет диагностическую визуализацию с последующей нелучевой терапией любого типа, включая, конечно, химиотерапию, а также хирургию (с визуальным контролем) и дистанционную радиотерапию. Благодаря этому, тераностика в будущем снизит расходы системы здравоохранения, ограничив назначение дорогих препаратов и методов лечения только тем пациентам, которым они действительно помогут.
К 2011 году в разработке находились несколько препаратов для радиотераностики, но, к сожалению, бюджет этих исследований был ограничен и не позволял провести финальную стадию испытаний. Только компании ААА с ее NET терапией, использующей молекулу 177Lu-DOTATATE, удалось дойти до конца, вложив значительные средства.
Крупные фармацевтические компании стали проявлять интерес к исследованиям молекул только, когда стало понятно, что FDA не выпустит на рынок молекулы, эффективные для ограниченного числа пациентов, с тем, чтобы, за неимением альтернативных вариантов, они назначались всем больным, даже тем, кому не помогут. Компания Bayer первой вложила крупные средства в препарат с мечеными радиоизотопами (223Ra-Xofigo), предназначенный для лечения пациентов с кастрационно-резистентным раком предстательной железы, симптоматическими метастазами в кости и метастазами во внутренние органы. И, хотя этот препарат не считается средством радиотераностики, колоссальный потенциал этой молекулы вызвал интерес у других компаний. Novartis потратила несколько миллиардов на приобретение двух других молекул – 177Lu-DOTATATE, которая вышла на рынок известна под названием Lutathera, и 177Lu-PSMA-617, предназначенная для лечения метастатического рака предстательной железы, выход которой на рынок запланирован на 2021 год. Обе молекулы работают в паре со своим аналогом, предназначенным для диагностики и отбора пациентов, имеющим в своем составе меченный радионуклид Gallium-68 для ПЭТ визуализации.
Такой успех запустил гонку за препаратами с мечеными радионуклидами, и на сегодняшний день более половины крупнейших фармацевтических компаний либо приобрели соответствующие активы в этой области, либо ведут разработку веществ с мечеными радионуклидами. Это такие компании, как Roche, J&J, Astra Zeneca, GSK, Merck, Pfizer и др. Кроме того, за последние три года появились новые игроки, такие как Telix Pharmaceuticals, занимающиеся исключительно разработкой препаратов для радиотераностики. Сегодня в этой области работает более 20 молодых компаний, основанных в период с 2018 года и имеющих все возможности стать второй ААА.
Все лекарственные (радиотерапевтические) препараты связаны со своими диагностическим эквивалентами, и в настоящее время они охватывают практически все показания. Сейчас 28 молекул проходят клинические испытания, а их выход на рынок запланирован на 2026 год. Большая часть из них основана на 177Lu, и, как правило, работают в паре с 18F, 68Ga или 89Zr для диагностической визуализации. Самый последний тренд состоит в использовании альфа-излучателей, таких как Actinium-225: он с легкостью может заменить в той же молекуле 177Lu, но при этом имеет большую эффективность. Либо же его можно использовать в качестве альтернативы 177Lu для пациентов, имеющих плохой ответ на лечение. Сейчас опробуется новый подход – тандемная терапия, смысл которой заключается в одновременном введении препаратов, содержащих меченые радионуклиды 225Ac- и 177Lu.
За последнее десятилетие тераностика шагнула далеко вперед, и, как ожидается, большое количество парных препаратов вскоре поступят на рынок. Но для того, чтобы как можно больше врачей, онкологов и общественности узнали об этом новом методе лечения, предстоит сделать еще очень много.
Об авторе:
Ричард Зиммерман, президент и основатель фонда Oncidium и один из основателей MEDraysintell. Фонд Oncidium занимается продвижением радиотераностики для лечения рака и оказывает поддержку по более широкому внедрению этой инновационной и спасательной технологии по всему миру.
Оригинал статьи можно прочитать здесь