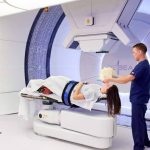
Флэш-терапия: загадочное оружие против рака
Исследователи из Института Кюри в Орсе, Франция вошли в историю в 2014 году как первооткрыватели флэш-терапии – метода лучевой терапии, позволяющего доставлять в мишень большие дозы радиации за доли секунды. Облучив грудные клетки лабораторных мышей короткими импульсами с дозами мощностью более 40 Грей в секунду, ученые наблюдали за подопытными животными в течение шести месяцев, отслеживая признаки фиброгенеза легких (образования рубцов под воздействием радиации). И пришли к выводу: нормальные, здоровые ткани при флэш-терапии получают гораздо меньше повреждений, чем при обычном облучении. Казалось бы, найден ответ на ключевой вопрос лучевой терапии: как убить опухоль, не навредив пациенту? Но почему флэш-терапия «умеет» это делать, ученые пока не знают.
Почему здоровые ткани не «видят» дозу?
«Мы используем однократную лечебную дозу, а это означает, что все лечение проводится сразу на одном участке за одну короткую последовательность», – сказал д-р Венсан Фаводон, разработчик этой методики.
Высокая скорость доставки доз в ходе флэш-терапии помогает уменьшить вред, причиняемый здоровой ткани, окружающей опухоль. Лечение рака по этой методике за один или несколько сеансов, как ожидается, значительно повысит эффективность процедур, снизит побочные эффекты, а заодно повысит пропускную способность больницы. Ведь в случае успеха пациентов будут лечить за доли секунды, а не за семь недель, с меньшим количеством осложнений, вызванных радиацией, и с очень высокой вероятностью получить контроль над опухолью.
«Дилемма применения лучевой терапии зачастую заключается в том, что во многих случаях опухоли физически не отделены от критических нормальных органов. Они как бы «вплетены» в них, – сказал д-р Билли Лу, профессор радиационной онкологии в Стэнфордском университете. – Даже очень тщательно формируя контуры дозы, вы все равно будете ограничены в ее повышении до необходимого для разрушения раковых клеток максимума, потому что нормальные ткани находятся прямо рядом с опухолью. С флэш-терапией мы разрабатываем стратегии как для создания высокоточных контуров доз, так и для их доставки за очень короткое время, чтобы максимально защитить нормальные ткани от воздействия радиации».
Большая часть научных изысканий с использованием флэш-терапии до сих пор проводилась в ходе доклинических исследований. Однако недавно начались первые клинические испытания на людях. Для экспериментов чаще всего используются электроны, хотя в некоторых случаях были применены протоны и рентгеновское излучение синхротронов.
«Флэш-терапия не обязательно минимизирует необходимую физическую дозу, попадающую на нормальную ткань, но, когда дозы излучения доставляются на очень высоких скоростях, здоровые ткани как бы не «видят» их, – сказал д-р Желько Вуякович, профессор радиационной онкологии в школе медицины Университета Мэриленда. – Вред от этого «флэш-эффекта» для нормальной ткани, по крайней мере, на основании некоторой доклинической работы, будет меньше, чем при стандартной протонной или фотонной терапии. Механизм, лежащий в основе этого явления, пока остается неясным».
Быстрее дыхания
Скорость и специфичность флэш-терапии делают ее особенно перспективной для облучения движущихся опухолей. Например, при лучевой терапии рака легких лечение должно проводиться с синхронизацией пучка частиц с дыхательным циклом.
«Это был один из первоначальных мотивов разработки сверхбыстрого метода лучевой терапии, – говорит Лу. – Если мы сможем доставлять дозу в мишень почти мгновенно, тогда облучение будет «опережать» движения тела. Это позволит нам доставлять дозы облучения, точно повторяющие контуры опухоли, и при этом не подвергать риску здоровые ткани».
В апреле 2019 года Вуякович и его коллеги из отделения радиационной онкологии Университета Мэриленда представили результаты исследований по раку легких. Они были получены в ходе доклинических исследований с использованием протонной флэш-терапии. При использовании флэш-терапии ученые зафиксировали снижение повреждений легочной ткани (и, соответственно, уменьшение фиброзов) на 25-30 процентов, а дерматитов кожи – на 35 процентов.
В этом исследовании впервые в флэш-терапии были использованы протоны, а не электроны, и на выходе врачи получили значительное снижение повреждений легких. По утверждению Вуяковича, флэш-терапия с электронами в первую очередь подходит для поверхностных опухолей (например, рака кожи), тогда как протонной флэш-терапией можно лечить глубоко расположенные новообразования
Впереди долгий путь
Несмотря на потенциальные преимущества флэш-терапии, по-прежнему не решен ряд важных вопросов. Необходимы дальнейшие радио-биологические эксперименты для подтверждения того, что первичные результаты могут быть воспроизведены в различных условиях, а также – для оценки отдаленных последствий применения метода. Пока, подчеркивают ученые, непонятен механизм малого воздействия флеш-терапии на здоровые ткани и потому сложно спрогнозировать, что может произойти в организме пациента через 10-15 лет после ее применения.
Фракционирование – это еще одна область, в которой необходимы поиски дополнительной информации. «Первый вопрос: нужно ли фракционировать дозу облучения или нет. Второй вопрос: проводя всю процедуру всего за доли секунды, вы должны быть абсолютно уверены, что доставка дозы осуществляется правильно, для чего требуется очень тщательный контроль качества физики процесса облучения», – отмечает Билли Лу.
Внедрение флэш-терапии в клиническую практику потребует наличия более совершенного оборудования, поскольку существующие линейные ускорители не способны доставлять дозы радиации на требуемой скорости. Лу и его коллеги из Стэнфордского университета работают над этим в партнерстве с Национальной ускорительной лабораторией SLAC в рамках программы под названием PHASER.
Сам по себе вопрос внедрения флэш-терапии имеет две составляющее: помимо клинической эффективности, важна экономическая целесообразность. «Стоимость этого метода лечения должна быть снижена, и эта технология должна обеспечивать лучшую экономичность, компактность и совместимость с имеющимися инфраструктурами, чтобы вам не приходилось строить новые здания специально для размещения в них нового оборудования», – сказал Лу. Решение ключевых проблем поставит множество новых вопросов: доступность нового лечения для пациентов, подготовка персонала к применению новой технологии, изменение стандартов лечения и так далее.
Оригинал новости можно прочитать здесь